Ina Alsina 1, Ieva Erdberga 1*, MaraDuma 2, Reinis Alksnis3 und Laila Dubova 1
1 Landwirtschaftliche Fakultät, Institut für Boden- und Pflanzenwissenschaften, Lettische Universität für Biowissenschaften und Technologien, Jelgava, Lettland,
2 Department of Chemistry, Faculty of Food Technology, Latvia University of Life Sciences and Technologies, Jelgava, Lettland,
3 Institut für Mathematik, Fakultät für Informationstechnologien, Lettische Universität für Biowissenschaften und Technologien, Jelgava, Lettland
EINFÜHRUNG
Mit zunehmendem Verständnis für die Bedeutung der Ernährung für die Sicherung der Qualität und Nachhaltigkeit des menschlichen Lebens wächst der Druck auf den Agrarsektor als grundlegendes Element zur Sicherung der Lebensmittelqualität. Tomaten sind als das am zweithäufigsten angebaute Gemüse [laut Statistik der Ernährungs- und Landwirtschaftsorganisation (FAO) für 2019] ein wichtiger Bestandteil der Küche fast aller Nationen.
Die begrenzte Kalorienzufuhr, der relativ hohe Ballaststoffgehalt und das Vorhandensein von Mineralstoffen, Vitaminen und Phenolen wie Flavonoiden machen die Tomatenfrucht zu einem hervorragenden „funktionellen Lebensmittel“, das viele physiologische Vorteile und grundlegende Ernährungsbedürfnisse bietet (1). Die in Tomaten enthaltenen biochemisch aktiven Substanzen, hauptsächlich aufgrund ihrer hohen antioxidativen Kapazität, sind nicht nur für die allgemeine Verbesserung der Gesundheit, sondern auch als therapeutische Option gegen verschiedene Krankheiten wie Diabetes, Herzkrankheiten und Toxizitäten anerkannt (2-4). Reife Tomatenfrüchte enthalten durchschnittlich 3.0-8.88 % Trockenmasse, die aus 25 % Fructose, 22 % Glucose, 1 % Saccharose, 9 % Zitronensäure, 4 % Äpfelsäure, 8 % Mineralstoffen, 8 % Protein, 7 % Pektin besteht , 6 % Zellulose, 4 % Hemizellulose, 2 % Lipide und die restlichen 4 % sind Aminosäuren, Vitamine, Phenolverbindungen und Pigmente (5, 6). Die Zusammensetzung dieser Verbindungen variiert je nach Genotyp, Wachstumsbedingungen und Fruchtentwicklungsstadium. Tomatenpflanzen reagieren sehr empfindlich auf Umweltfaktoren wie Lichtverhältnisse, Temperatur und die Wassermenge im Substrat, die zu Veränderungen im Pflanzenstoffwechsel führen, die wiederum die Qualität und chemische Zusammensetzung der Früchte beeinflussen (7). Umweltbedingungen beeinflussen sowohl die Tomatenphysiologie als auch die Synthese von Sekundärmetaboliten. Pflanzen, die unter Stressbedingungen wachsen, reagieren darauf, indem sie ihre antioxidativen Eigenschaften erhöhen (8).
Der Ursprung der Tomatenart ist mit der zentralamerikanischen Region verbunden (9) und Techniken wie der Bau von Gewächshäusern zur Bereitstellung der notwendigen Temperatur und des Lichts für Tomaten sind häufig erforderlich, um die erforderlichen agroklimatischen Bedingungen zu schaffen, insbesondere in der gemäßigten Klimazone und während der Wintersaison. Unter solchen Bedingungen ist Licht oft der limitierende Faktor für die Tomatenentwicklung. Zusätzliche Beleuchtung während der Winter- und Frühjahrssaison ermöglicht die Produktion hochwertiger Tomaten während der Zeit mit geringer Sonneneinstrahlung
(10) . Der Einsatz von Lampen mit unterschiedlichen Wellenlängen kann nicht nur für einen ausreichenden Tomatenertrag sorgen, sondern auch die biochemische Zusammensetzung der Tomatenfrucht verändern. In der Gewächshausindustrie werden seit 60 Jahren Natriumdampf-Hochdrucklampen (HPSL) aufgrund ihrer langen Lebensdauer und geringen Anschaffungskosten eingesetzt
(11) . In den letzten Jahren haben sich jedoch Leuchtdioden (LEDs) als energiesparendere Alternative immer mehr durchgesetzt (12). Zusätzliche LED wurde als effiziente Lichtquelle verwendet, um die Nachfrage für die Tomatenproduktion zu decken. Der Lycopin- und Luteingehalt in Tomaten war um 18 und 142 % höher, wenn sie der zusätzlichen LED-Beleuchtung ausgesetzt waren. Jedoch, в-Carotingehalt unterschied sich nicht zwischen den Lichtbehandlungen (12). LED blaues und rotes Licht erhöht Lycopin und в-Carotingehalt (13), was zu einer frühen Reifung der Tomatenfrucht führt (14). Lösliche Zuckergehalte der reifen Tomatenfrucht wurden durch längere Dauer von dunkelrotem (FR) Licht verringert (15). Analoge Schlussfolgerungen wurden in der Studie von Xie gezogen: Rotes Licht induziert eine Anhäufung von Lycopin, aber FR-Licht kehrt diesen Effekt um (13). Es gibt weniger Informationen über die Auswirkungen von blauem Licht auf die Entwicklung von Tomatenfrüchten, aber Studien zeigen, dass blaues Licht einen geringeren Einfluss auf die Menge an biochemischen Verbindungen in Tomatenfrüchten hat, aber mehr auf die Prozessstabilität. Zum Beispiel haben Kong und andere herausgefunden, dass blaues Licht besser verwendet werden kann, um die Haltbarkeit von Tomaten zu verlängern, da blaues Licht die Festigkeit der Frucht deutlich erhöht (16), was im Wesentlichen bedeutet, dass blaues Licht den Reifungsprozess verlangsamt, was zu einer Erhöhung der Menge an Zucker und Pigmenten führt. Ein ähnliches Muster zeigt der Einsatz von Gewächshausabdeckungen zur Regulierung der Lichtzusammensetzung. Die Verwendung einer Beschichtung mit einer höheren Rot- und einer niedrigeren Blaulichtdurchlässigkeit erhöht den Lycopingehalt um etwa 25 %. In Kombination mit einer von 11 auf 12 h erhöhten Photoperiode erhöht sich die Menge an Lycopin um ca. 70 % (17). In Studien ist es nicht immer möglich, die Wirkung von Faktoren auf Änderungen in der chemischen Zusammensetzung von Tomatenfrüchten genau zu unterscheiden. Insbesondere unter Gewächshausbedingungen kann die Zusammensetzung der Früchte durch erhöhte Temperaturen oder reduzierte Wassermengen erhöht werden. Darüber hinaus können diese Faktoren mit dem Genotyp korrelieren, der für die Sorte und das Entwicklungsstadium spezifisch ist (1, 18). Ein Wasserdefizit kann die Qualität von Tomatenfrüchten aufgrund erhöhter Gehalte an löslichen Feststoffen (Zucker, Aminosäuren und organische Säuren) verbessern, bei denen es sich um Hauptverbindungen handelt, die sich in Früchten ansammeln. Ein Anstieg löslicher Feststoffe verbessert die Qualität von Früchten, da er das Aroma und den Geschmack beeinflusst (8).
Trotz der berichteten Auswirkungen des Lichtspektrums auf die Akkumulation von Pflanzenmetaboliten ist ein breiteres Wissen über verschiedene Spektraleffekte zur Verbesserung der Qualität von Tomaten erforderlich. Dementsprechend ist das Ziel dieser Studie, die Wirkung einer zusätzlichen Beleuchtung im Gewächshaus auf die Akkumulation von Primär- und Sekundärmetaboliten in verschiedenen Tomatensorten zu bewerten. Änderungen des spektralen Inhalts des Beleuchtungssystems können die Zusammensetzung von Primär- und Sekundärmetaboliten in Tomatenfrüchten verändern. Das erworbene Wissen verbessert das Verständnis der Wirkung von Licht auf den Zusammenhang zwischen Ertrag und dessen Qualität.
Material und Methoden
Pflanzenmaterial und Wachstumsbedingungen Die Experimente wurden im Gewächshaus (Polykarbonat mit 4-mm-Zellen) des Instituts für Boden- und Pflanzenwissenschaften der Lettischen Universität für Biowissenschaften und Technologien 56 durchgeführt°39'N 23°43'E in den Saisons 2018/2019, 2019/2020 und 2020/2021 vom Spätherbst bis zum frühen Frühling.
Kommerziell gepfropfte Tomatensorten (Solanum lycopersicum L.) „Bolzano F1“ (Fruchtfarbe – orange), „Chocomate F1“ (Fruchtfarbe – rotbraun) und rote Fruchtsorten „Diamont F1“, „Encore F1“ und „ Strabena F1“ verwendet. Jede Pflanze hatte zwei führende Köpfe und wurde während des Wachstums auf einem Hochseilsystem gerüstet. Die erhaltenen Pflanzen wurden zunächst in schwarze 5-l-Plastikbehälter mit "Laflora"-Torfsubstrat KKS-2, pH umgepflanztKCl 5.2–6.0 und Fraktionsgröße 0–20 mm, PG-Gemisch (NPK 15–1020) 1.2 kg m-3, Ca 1.78 % und Mg 0.21 %. Als die Pflanzen die Blüte erreichten, wurden sie in schwarze 15-l-Plastikbehälter mit dem gleichen „Laflora“-Torfsubstrat KKS-2 umgepflanzt. Die Pflanzen wurden während der vegetativen Phase des Pflanzenwachstums einmal pro Woche mit einer 1%igen Lösung von Kristalon Green (NPK 18-18-18) mit Mg, S und Mikroelementen und mit Kristalon Red (NPK 12-12-36) mit Mikroelementen oder 1 gedüngt % Ca(NO3)2 während der Fortpflanzungsphase im Verhältnis 300 ml pro Liter Substrat.
Der Wassergehalt in den Vegetationsbehältern wurde bei 50–80 % der vollen Wasserhaltekapazität gehalten. Die durchschnittlichen Tages-/Nachttemperaturen waren 20-22°C/17-18°C.
Die maximale Temperatur während des Tages (März) hat 32 nicht überschritten°C und minimale Temperatur (November) während der Nacht war es nicht <12°Die Temperatur wurde auch unter den Lampen im Abstand von 50, 100 und 150 cm von der Leuchte gemessen. Es wurde festgestellt, dass die Temperatur unter der HPSL 50 cm von der Leuchte entfernt 1.5 betrug°C höher als unter den anderen. Temperaturunterschiede auf Fruchtebene wurden nicht festgestellt.
Lichtverhältnisse
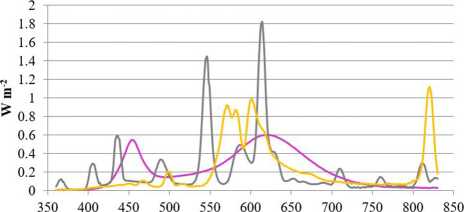
Tomaten wurden in der Herbst-Frühlings-Saison kultiviert, indem zusätzliche Beleuchtung mit einer Lichtperiode von 16 h verwendet wurde. Es wurden drei verschiedene Lichtquellen verwendet: Led Cob Helle Top LED 280 (LED), Induktionslampe (IND) und HPSL Helle Magna (HPSL). Auf der Scheitelhöhe erhielten die Pflanzen 200 ± 30 ^mol m-2 s-1 unter LED und HPSL und 170 ± 30 ^mol m-2 s-1 unter IND-Lampen. Die Verteilung der Lichtstrahlung ist in dargestelltFiguren 1,2. Lichtintensität und spektrale Verteilung wurden mit dem tragbaren Spektrallichtmeter MSC15 (Gigahertz Optik GmbH, Türkenfeld, Deutschland, UK) erfasst.
Die verwendeten Lampen unterschieden sich in ihrer spektralen Lichtverteilung. Dem Sonnenlicht im roten Teil (625–700 nm) des Spektrums am ähnlichsten war HPSL. Die IND-Lampe in diesem Teil des Spektrums gab 23.5 % weniger Licht ab, aber LED war fast doppelt so hell. Orangefarbenes Licht (2–590 nm) wurde hauptsächlich von HPSL emittiert, grünes Licht (625–500 nm) wurde hauptsächlich von IND emittiert, blaues Licht (565–450 nm) wurde hauptsächlich von LED emittiert, aber violettes Licht (485 nm) wurde emittiert hauptsächlich von IND-Lampen emittiert. Beim Vergleich des gesamten Spektrums des sichtbaren Lichts sollte die LED-Lichtquelle als dem Sonnenlicht am nächsten und die IND als die ungeeignetste in Bezug auf das Spektrum betrachtet werden.
Extraktion und Bestimmung von sekundären Pflanzenstoffen
Tomatenfrüchte wurden im Vollreifestadium geerntet. Die Früchte wurden einmal im Monat geerntet, beginnend Mitte November und endend im März. Alle Früchte wurden gezählt und gewogen. Mindestens 5 Früchte von jeder Variante (für cv „Strabena“ – 8–10 Früchte) wurden für Analysen beprobt. Tomatenfrüchte wurden unter Verwendung eines Handmixers zu einem Püree gemahlen. Für jeden bewerteten Parameter wurden drei Wiederholungen analysiert.
Bestimmung von Lycopin u в-Carotin
Zur Bestimmung der Konzentration von Lycopin u в-Carotin wurde dann eine Probe von 0.5 ± 0.001 g aus dem Tomatenpüree in ein Röhrchen eingewogen und 10 ml Tetrahydrofuran (THF) wurden zugegeben (19). Die Röhrchen wurden verschlossen und für 15 min bei Raumtemperatur gehalten, gelegentlich geschüttelt und schließlich für 10 min bei 5,000 U/min zentrifugiert. Die Extinktion der erhaltenen Überstände wurde spektrophotometrisch bestimmt, indem die Extinktion bei 663, 645, 505 und 453 nm und dann das Lycopin und gemessen wurden в-Carotingehalt (mg 100 ml-1) wurden gemäß der folgenden Gleichung berechnet.
CLyc = -0.0458 x Àббз + 0.204 x Àb45 + 0.372 x A505– 0.0806 x A453 (1)
CAuto = 0.216 x A663 – 1.22 x A645 – 0.304 x A505+ 0.452 x A453 (2)
wobei A663, A645, A505 und A453 – Absorption bei entsprechender Wellenlänge (20).
Das Lycopin u в-Carotinkonzentrationen werden in mg g ausgedrücktF-M1 .
Bestimmung der Gesamtphenole
Eine Probe von 1 ± 0.001 g des Tomatenpürees wurde in ein graduiertes Röhrchen eingewogen und 10 ml Lösungsmittel (Methanol/destilliertes Wasser/Salzsäure 79:20:1) wurden zugegeben. Die graduierten Röhrchen wurden verschlossen und 60 min bei 20°C geschüttelt°C im Dunkeln gewaschen und anschließend 10 min bei 5,000 U/min zentrifugiert. Die Gesamtphenolkonzentration wurde unter Verwendung des spektrophotometrischen Folin-Ciocalteu-Verfahrens bestimmt (21) mit einigen Modifikationen: Folin-Ciocalteu-Reagenz (10-fach in destilliertem Wasser verdünnt) wurde zu 0.5 ml des Extrakts gegeben und nach 3 min wurden 2 ml Natriumcarbonat (Na2CO3) (75 gL-1). Die Probe wurde gemischt und nach 2 h Inkubation bei Raumtemperatur im Dunkeln wurde die Extinktion bei 760 nm gemessen. Die Konzentration der gesamten phenolischen Verbindungen wurde unter Verwendung der Eichkurve und der erhaltenen Gleichung 3 berechnet und als Gallussäureäquivalent (GAE) pro 100 g frischer Tomatenmasse ausgedrückt.
0.556 x (A760 + 0.09) x 100
Phe = 0.556 × (A760 + 0.09) × 100/m (3)
wo ein760-Absorption bei entsprechender Wellenlänge und m— Masse der Probe.
Bestimmung von Flavonoiden
Eine Probe von 1 ± 0.001 g des Tomatenpürees wurde in ein graduiertes Röhrchen eingewogen und 10 ml Ethanol wurden hinzugefügt. Die graduierten Röhrchen wurden verschlossen und 60 min bei 20°C geschütteltoC im Dunkeln gewaschen und anschließend 10 min bei 5,000 U/min zentrifugiert. Die kolorimetrische Methode (22) wurde verwendet, um Flavonoide mit geringfügigen Veränderungen zu bestimmen: 2 ml destilliertes Wasser und 0.15 ml 5% Natriumnitrit (NaNO2)-Lösung wurden zu 0.5 ml des Extrakts gegeben. Nach 5 min werden 0.15 ml einer 10 %igen Aluminiumchloridlösung (AlCl3) wurde hinzugefügt. Das Gemisch wurde weitere 5 min stehengelassen und 1 ml 1 M Natriumhydroxid (NaOH)-Lösung wurde zugegeben. Die Probe wurde gemischt und nach 15 min bei Raumtemperatur wurde die Extinktion bei 415 nm gemessen. Die Flavonoid-Gesamtkonzentration wurde unter Verwendung der Eichkurve und Gleichung 4 berechnet und als Menge an Catechin-Äquivalenten (CEs) pro 100 g frischem Tomatengewicht ausgedrückt.
Fla = 0.444 × A415 × 100/m (4)
wo ein415-Absorption bei entsprechender Wellenlänge und m— Masse der Probe.
Bestimmung von Trockenmasse und löslichen Feststoffen Die Trockenmasse wurde bestimmt, indem Proben im Thermostat bei 60 getrocknet wurdenoC.
Der Gesamtgehalt an löslichen Feststoffen (ausgedrückt als ◦Brix) wurde mit einem auf 301 kalibrierten Refraktometer (A.KRUSS Optronic Digital Handheld Refractometer Dr95-20) gemessenoC mit destilliertem Wasser.
Bestimmung der titrierbaren Säure (TA)
Eine Probe von 2 ± 0.01 g des Tomatenpürees wurde in ein graduiertes Röhrchen eingewogen und mit destilliertem Wasser bis auf 20 ml versetzt. Die graduierten Röhrchen wurden verschlossen und 60 min bei Raumtemperatur geschüttelt und dann 10 min bei 5,000 U/min zentrifugiert. 5-ml-Aliquots wurden mit 0.1 M NaOH in Gegenwart von Phenolphthalein titriert.
TA = VNaOH × Vt/Vs × m (5)
wo V.NaoH-Volumen der verwendeten 0.1 M NaOH, Vt – Gesamtvolumen (20 ml) und Vs – Probenvolumen (5 ml).
Die Ergebnisse werden als mg Zitronensäure pro 100 g frischem Tomatengewicht ausgedrückt. 1 ml 0.1 M NaOH entspricht 6.4 mg Zitronensäure.
Bestimmung des Geschmacksindex (TI)
Ein TI wurde unter Verwendung von Gleichung 6 berechnet (23).
TI = ◦Brix/(20 × TA)+ TA (6)
Statistische Analysen
Die Normalität und Homogenität der deskriptiven Statistik wurde für 354 Beobachtungen getestet. Der Shapiro-Wilk-Test wurde zur Bewertung der Normalität innerhalb jeder Kombination aus Sorte und Lichtbehandlung verwendet. Um die Homogenität der Varianzen abzuschätzen, wurde der Levene-Test durchgeführt. Der Kruskal-Wallis-Test wurde verwendet, um die Unterschiede zwischen den Lichtverhältnissen zu untersuchen. Wenn statistisch signifikante Unterschiede festgestellt wurden, wurde der Wilcoxon-Post-Hoc-Test mit Bonferroni-Korrekturen für paarweise Vergleiche verwendet. Das im Text, in den Tabellen und Grafiken verwendete Signifikanzniveau ist a = 5 %, sofern nicht anders angegeben.
ERGEBNISSE
Tomatenfruchtgröße und biochemische Parameter der Frucht sind genetisch bedingte Parameter, aber die Anbaubedingungen haben einen signifikanten Einfluss auf diese Merkmale. Die größten Früchte werden von „Diamont“ (88.3 ± 22.9 g) und die kleinsten Früchte von „Strabena“ (13.0 ± 3.8 g) geerntet, einer Sorte von Kirschtomaten. Auch die Größe der Früchte innerhalb der Sorte variierte je nach Erntezeitpunkt. Die größten Früchte wurden zu Beginn der Produktion geerntet und die Größe der Tomaten nahm mit dem Wachstum der Pflanzen ab. Allerdings ist zu beachten, dass mit dem erhöhten Anteil an natürlichem Licht Ende März die Tomatengröße leicht zugenommen hat.
In allen drei Jahren wurde der höchste Tomatenertrag mit HPSL als Zusatzbeleuchtung geerntet. Der Ertragsrückgang bei LEDs betrug 16.0 % und bei IND – 17.7 % im Vergleich zu HPSL. Verschiedene Tomatensorten reagierten unterschiedlich auf zusätzliche Beleuchtung. Bei den Sorten „Strabena“, „Chocomate“ und „Diamont“ wurden unter LEDs zwar statistisch unbedeutende Ertragssteigerungen beobachtet. Für CV „Bozen“ war weder LED- noch IND-Zusatzbeleuchtung geeignet, es wurde eine Minderung des Gesamtertrags um 25-31% beobachtet.
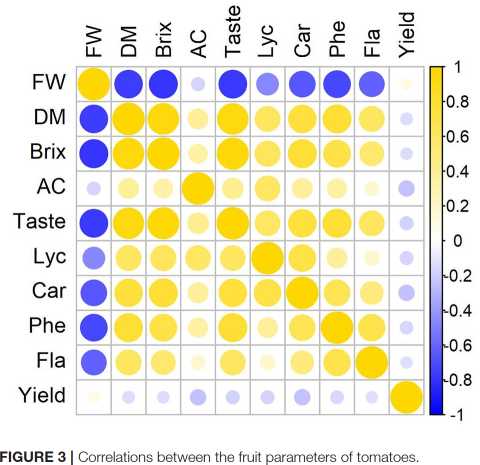
Größere Tomatenfrüchte enthalten im Durchschnitt weniger Trockenmasse und lösliche Feststoffe, sie sind nicht so schmackhaft und enthalten weniger Carotinoide und Phenole. Der Faktor, der am wenigsten von der Fruchtgröße beeinflusst wird, ist der Säuregehalt. Es wird eine hohe Korrelation zwischen dem Gehalt an Trockenmasse und löslichen Feststoffen und dem TI (rn=195 > 0.9). Der Korrelationskoeffizient zwischen dem Trockensubstanz- bzw. Trockensubstanzgehalt und dem Carotinoid (Lycopin und Carotin) und dem Phenolgehalt liegt zwischen 0.7 und 0.8 (Figure 3).
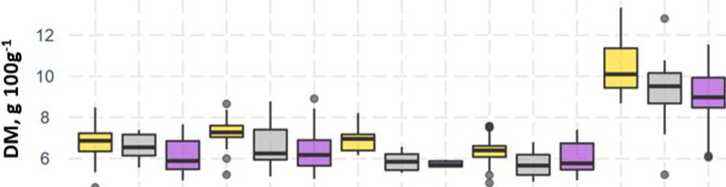
Experimente haben gezeigt, dass, obwohl die Unterschiede in den untersuchten Parametern zwischen den verwendeten Lichtern manchmal groß sind, es wenige solche Parameter gibt, die sich unter dem Einfluss der verwendeten Lichtquelle während der gesamten Vegetationsperiode und unter Berücksichtigung der Sorte und drei signifikant ändern würden Vegetationsperioden (Tabelle 1). Es kann festgestellt werden, dass Tomaten aller unter HPSL angebauten Sorten mehr Trockenmasse aufweisen (Tabelle 1undFigure 5).
Frischgewicht, Trockenmasse und lösliche Feststoffe
Gewicht und Größe der Früchte hängen maßgeblich von den Wachstumsbedingungen der Pflanze ab. Obwohl es Unterschiede zwischen den Sorten gab, war die durchschnittliche Frucht von Tomaten, die unter Induktionslampen wuchsen, 12 % kleiner als unter HPSL oder LED. Verschiedene Sorten scheinen unterschiedlich auf das zusätzliche LED-Licht zu reagieren. Größere Früchte werden unter den LEDs von „Chocomate“ und „Diamont“ gebildet, aber das Frischgewicht von „Bolzano“ beträgt im Durchschnitt nur 72 % des Gewichts von Tomaten unter HPSL. Früchte von „Encore“ und „Strabena“, die unter LED- und IND-Zusatzbeleuchtung angebaut werden, haben ein ähnliches Gewicht und sind 10 bzw. 7 % kleiner als Tomaten, die unter HPSL angebaut werden (Figure 4).
Der Trockenmassegehalt ist einer der Indikatoren für die Fruchtqualität. Er korreliert mit dem Gehalt an löslichen Trockensubstanzen und beeinflusst den Geschmack von Tomaten. In unseren Versuchen variierte der Trockensubstanzgehalt von Tomaten zwischen 46 und 113 mg g-1. Der höchste Trockenmassegehalt (durchschnittlich 95 mg g-1) wurde für die Kirschsorte „Strabena“ gefunden. Unter anderen Tomatensorten ist der höchste Trockenmassegehalt (durchschnittlich 66 mg g-1) wurde in „Chocomate“ gefunden (Figure 5).
Während des Experiments lag der Gehalt an organischer Säure, ausgedrückt als Zitronensäure (CA)-Äquivalent in Tomaten, im Durchschnitt zwischen 365 und 640 mg 100 g-1 . Der höchste Gehalt an organischen Säuren wurde in der Kirschtomate cv „Strabena“ gefunden, durchschnittlich 596 ± 201 mg CA 100 g-1, aber der niedrigste Gehalt an organischen Säuren wurde in der gelben Fruchtsorte „Bolzano“ gefunden, durchschnittlich 545 ± 145 mg CA 100 g-1. Der Gehalt an organischen Säuren variierte nicht nur zwischen den Sorten, sondern auch zwischen den Probenahmezeitpunkten stark; Im Durchschnitt wurde jedoch ein höherer Gehalt an organischen Säuren in Tomaten gefunden, die unter IND-Lampen angebaut wurden (wobei HPSL und LED um 10.2 % übertroffen wurden).
Im Durchschnitt wurde der höchste Trockenmassegehalt in Früchten gefunden, die unter HPSL angebaut wurden. Unter der IND-Lampe sinkt der Trockensubstanzgehalt von Tomatenfrüchten um 4.7-16.1%, unter der LED von 9.9-18.2%. Die in den Versuchen verwendeten Sorten sind unterschiedlich lichtempfindlich. Die geringste Abnahme der Trockenmasse unter verschiedenen Lichtbedingungen wurde für die Sorte „Strabena“ (5.8 % für IND bzw. 11.1 % für LED) und die größte Abnahme der Trockenmasse unter verschiedenen Lichtbedingungen für die Sorte „Diamont“ (16.1 % und 18.2 XNUMX %).
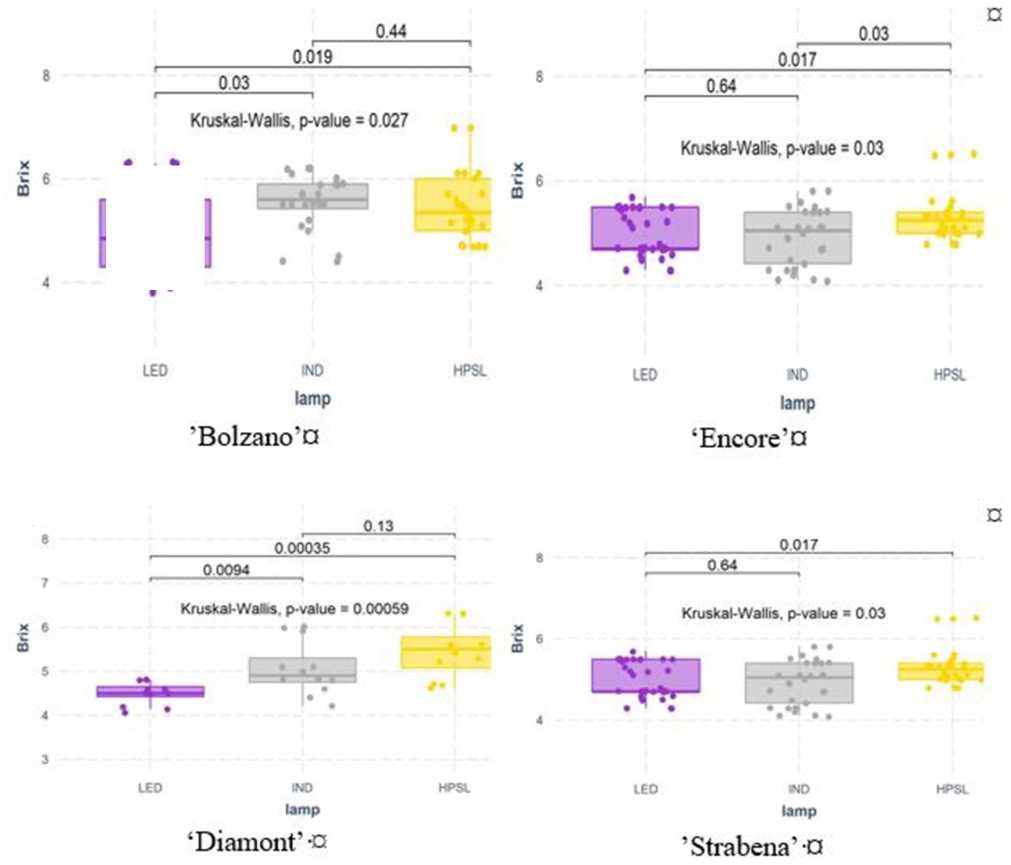
Im Durchschnitt variierte der Gehalt an löslichen Feststoffen zwischen 3.8 und 10.2 ◦Brix. In ähnlicher Weise wurde für die Trockenmasse der höchste Gehalt an löslichen Feststoffen in der Kirschtomatensorte „Strabena“ nachgewiesen (im Durchschnitt 8.1 ± 1.0 ◦Brix). Die Tomatensorte „Diamont“ war am wenigsten süß (im Durchschnitt 4.9 ± 0.4 ◦Brix).
Zusätzliche Beleuchtung beeinflusste den Gehalt an löslichen Feststoffen der Tomatensorten „Bolzano“, „Diamont“ und „Encore“ erheblich. Unter LED-Licht nahm der Gehalt an löslichen Feststoffen bei diesen Sorten im Vergleich zu HPSL deutlich ab. Die Wirkung der IND-Lampe war geringer. Unter diesen Lichtbedingungen wiesen wachsende Tomaten der Sorten „Bolzano“ und „Strabena“ im Durchschnitt 4.7 bzw. 4.3 % mehr Zucker auf als unter HPSL angebaut. Leider ist dieser Anstieg statistisch nicht signifikant (Figure 6).
Tomaten TI variiert von 0.97 bis 1.38. Am schmackhaftesten waren Tomaten der Sorte „Strabena“, im Durchschnitt betrug der TI 1.32 ± 0.1, und am schlechtesten waren Tomaten der Sorte „Diamont“, im Durchschnitt betrug der TI nur 1.01 ± 0.06. Hoher TI hat die Tomatensorte „Bolzano“ mit einem durchschnittlichen TI (1.12 ± 0.06), gefolgt von „Chocomate“ mit einem durchschnittlichen TI (1.08 ± 0.06).
Im Durchschnitt wird der TI nicht wesentlich von der Lichtquelle beeinflusst, außer bei der Sorte „Strabena“, wo die Früchte unter einer IND-Lampe stehen
TABELLE 1 | P-Werte (Kruskal-Wallis-Test) der Auswirkungen verschiedener Zusatzbeleuchtungen auf die Tomatenfruchtqualität (n = 118).
|
Parameter |
„Bozen“ |
„Schokolade“ |
"Zugabe" |
„Diamant“ |
„Strabena |
|
Fruchtgewicht |
0.013 * |
0.008 ** |
0.110 |
0.400 |
0.560 |
|
Trockenmasse |
0.022 * |
0.013 * |
0.011 * |
0.001 ** |
0.015 * |
|
Lösliche Feststoffe |
0.027 * |
0.030 |
0.030 * |
0.001 ** |
0.270 |
|
Säure |
0.078 |
0.022 |
0.160 |
0.001 ** |
0.230 |
|
Geschmacksindex |
0.370 |
0.140 |
0.600 |
0.001 ** |
0.023 * |
|
Lycopin |
0.052 |
0.290 |
0.860 |
0.160 |
0.920 |
|
в-Carotin |
<0.001 *** |
0.007 ** |
0.940 |
0.110 |
0.700 |
|
Phenole |
0.097 |
0.750 |
0.450 |
0.800 |
0.420 |
|
Flavonoide |
0.430 |
0.035 * |
0.720 |
0.440 |
0.170 |
| Signifikanzniveaus „* **„0.001“,**” 0.01 und “*"0.05. |
|
So wurde beim TI Anstieg im Vergleich zu HPSL um 7.4 % (LED um 4.2 %) im Vergleich zu HPSL und CV „Diamont“ unter beiden zuvor genannten Lichtbedingungen eine Abnahme um 5.3 bzw. 8.4 % festgestellt.
Gehalt an Carotinoiden
Die Lycopinkonzentration in Tomaten variierte von 0.07 (CV „Bolzano“) bis 7 mg 100 g-1 FM („Strabena“). Etwas höherer Lycopingehalt im Vergleich zu „Diamont“ (4.40 ± 1.35 mg 100 g-1 FM) und „Encore“ (4.23 ± 1.33 mg 100 g-1 FM) wurde in bräunlich rot gefärbten Früchten von „Chocomate“ gefunden (4.74 ± 1.48 mg 100 g-1 UKW).
Im Durchschnitt enthalten Früchte von Pflanzen, die unter IND-Lampen angebaut wurden, 17.9 % mehr Lycopin im Vergleich zu HPSL. LED-Beleuchtung hat auch die Lycopin-Synthese gefördert, jedoch in geringerem Maße, nämlich um durchschnittlich 6.5 %. Die Wirkung von Lichtquellen ist je nach Sorte unterschiedlich. Die größten Unterschiede in der Lycopin-Biosynthese wurden bei „Chocomate“ beobachtet. Der Anstieg des Lycopingehalts unter IND im Vergleich zu HPSL betrug 27.2 % und unter LED 13.5 %. „Strabena“ war am wenigsten empfindlich mit Veränderungen von 3.2 bzw. -1.6 % im Vergleich zu HPSL (Figure 7). Trotz der relativ überzeugenden Ergebnisse bestätigt die mathematische Verarbeitung der Daten nicht deren Zuverlässigkeit (Tabelle 1).
Während des Experiments в-Carotingehalt in Tomaten im Durchschnitt von 4.69 bis 9.0 mg 100 g-1 FM. Das höchste в-Carotingehalt wurde in der Kirschtomate cv „Strabena“ im Durchschnitt von 8.88 ± 1.58 mg 100 g gefunden-1 FM, aber das niedrigste в-Carotin-Gehalt wurde in der gelben Fruchtsorte „Bozen“ mit durchschnittlich 5.45 ± 1.45 mg 100 g gefunden-1 FM
Die signifikanten Unterschiede im Carotingehalt wurden zwischen Sorten gefunden, die unter unterschiedlicher zusätzlicher Beleuchtung angebaut wurden. Die unter LED angebaute Cv „Bolzano“ zeigt einen signifikanten Rückgang des Carotingehalts (um 18.5 % im Vergleich zu HPSL), während „Chocomate“ den niedrigsten Carotingehalt knapp unter HPSL in Tomatenfrüchten aufweist (5.32 ± 1.08 mg 100 g FM-1) und wurde bei LED um 34.3 % und bei IND-Lampen um 46.4 % gesteigert (Figure 8).
Gesamtgehalt an Phenolen und Flavonoiden
Der Phenolgehalt von Tomatenfrüchten variiert im Durchschnitt zwischen 27.64 und 56.26 mg GAE 100 g-1 FM (Tabelle 2). Der höchste Phenolgehalt wird bei der Sorte „Strabena“ und der niedrigste Phenolgehalt bei der Sorte „Diamont“ beobachtet. Der Phenolgehalt von Tomaten schwankt je nach Reifezeit der Früchte, daher gibt es große Schwankungen zwischen verschiedenen Probenahmezeitpunkten. Dies führt dazu, dass die Unterschiede zwischen den unter verschiedenen Lampen angebauten Tomaten nicht signifikant sind.
Obwohl sich nur bei der Sorte „Chocomate“ signifikante Unterschiede zwischen den Zusatzlichtvarianten zeigen, ist der durchschnittliche Flavonoidgehalt von unter der Lampe gewachsenen Früchten um 33.3 %, unterhalb der LED jedoch um 13.3 % höher. Unter IND-Lampen werden große Unterschiede zwischen den Sorten beobachtet, aber unter LED liegt die Variabilität im Bereich von 10.3–15.6 %.
Versuche haben gezeigt, dass verschiedene Tomatensorten unterschiedlich auf die eingesetzte Zusatzbeleuchtung reagieren.
Es wird nicht empfohlen, die Sorte „Bolzano“ unter LED- oder IND-Lampen anzubauen, da bei dieser Beleuchtung die Parameter ähnlich wie bei HPSL oder deutlich niedriger sind. Unter LED-Lampen werden Gewicht einer Frucht, Trockenmasse, lösliche Feststoffe und Carotin deutlich reduziert ( Figure 9 ).
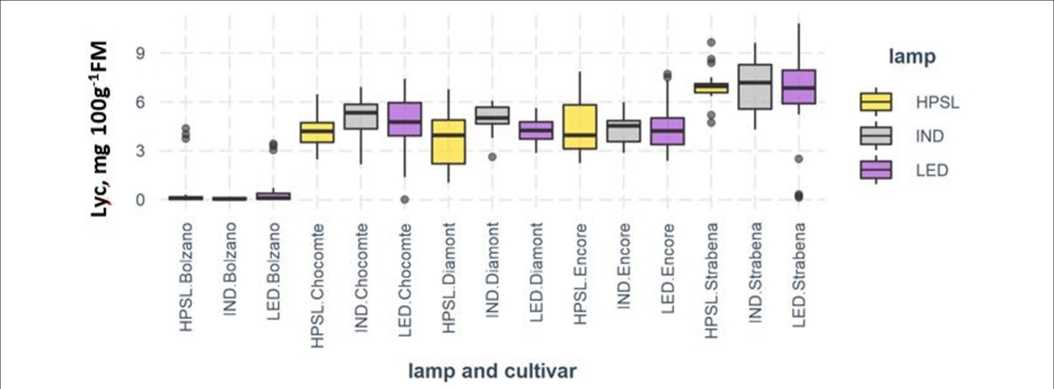
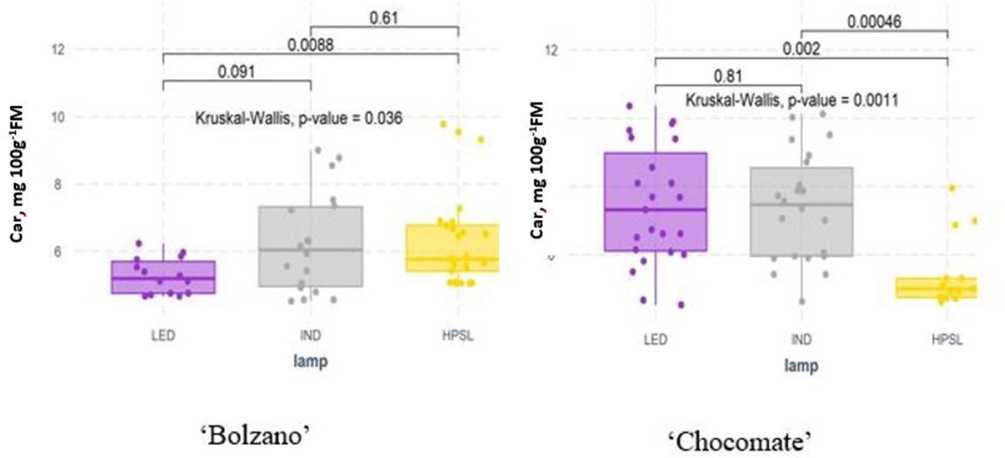
TABELLE 2 | Gehalt an Gesamtphenolen [mg Gallussäureäquivalent (GAE) 100 g-1 FM] und Flavonoide [mg Zitronensäure (CA) 100 g-1 FM] in den Tomatenfrüchten, die unter unterschiedlicher Zusatzbeleuchtung angebaut wurden.
|
Parameter |
„Bozen“ |
„Schokolade“ |
"Zugabe" |
„Diamant“ |
„Strabena“ |
|
Phenole |
|||||
|
HPSL |
36.33 ± 5.34 |
31.23 ± 5.67 |
27.64 ± 7.12 |
30.26 ± 5.71 |
48.70 ± 11.24 |
|
IND |
33.21 ± 4.05 |
34.77 ± 6.39 |
31.00 ± 6.02 |
30.63 ± 5.11 |
56.26 ± 13.59 |
|
LED |
36.16 ± 6.41 |
31.70 ± 6.80 |
30.44 ± 3.01 |
30.98 ± 6.52 |
52.57 ± 10.41 |
|
Flavonoide |
|||||
|
HPSL |
4.50 ± 1.32 |
3.78 ± 0.65a |
2.65 ± 1.04 |
2.57 ± 1.15 |
5.17 ± 2.33 |
|
IND |
4.57 ± 0.75 |
5.24 ± 0.79b |
4.96 ± 1.46 |
2.84 ± 0.67 |
6.65 ± 1.64 |
|
LED |
4.96 ± 1.08 |
4.37 ± 1.18ab |
3.02 ± 1.04 |
2.88 ± 1.08 |
5.91 ± 1.20 |
| Deutlich unterschiedliche Mittel sind mit unterschiedlichen Buchstaben gekennzeichnet. | |||||
Im Gegensatz zu „Bolzano“ erhöht „Chocomate“ unter LED-Beleuchtung das Gewicht einer Frucht und der Carotingehalt steigt. Andere Parameter, ausgenommen Trockenmasse und Gehalt an löslichen Feststoffen, sind ebenfalls höher als bei Früchten, die unter HPSL gewonnen wurden. Auch bei dieser Sorte zeigt die Induktionslampe gute Ergebnisse (Figure 9).
Bei der Sorte „Diamont“ werden die geschmacksbestimmenden Indikatoren unter LED-Licht deutlich reduziert, dafür aber der Gehalt an Pigmenten und Flavonoiden erhöht (Figure 9).
Die Sorten „Encore“ und „Strabena“ reagieren am wenigsten auf eine zusätzliche Lichtbehandlung. Bei „Encore“ ist der einzige Parameter, der signifikant vom LED-Lichtspektrum beeinflusst wird, der Gehalt an löslichen Feststoffen. „Strabena“ ist auch relativ tolerant gegenüber Änderungen in der spektralen Zusammensetzung des Lichts. Dies könnte auf die genetischen Eigenschaften der Sorte zurückzuführen sein, da dies die einzige Kirschtomatensorte war, die in den Versuch aufgenommen wurde. Es zeichnete sich durch deutlich höhere aller untersuchten Parameter aus. Änderungen der untersuchten Parameter unter Lichteinfluss konnten daher nicht festgestellt werden (Figure 9).
DISKUSSION
Das Durchschnittsgewicht der Tomatenfrucht korreliert mit dem beabsichtigten Gewicht der Sorte; es wird jedoch nicht erreicht. Dies könnte eher an der Anbaumethode als an der Qualität der Beleuchtung liegen, da in einem Torfsubstrat weniger Wasser verwendet werden kann, was das Gewicht der Früchte verringern kann, aber die Konzentration der Wirkstoffe erhöht und die Sättigung des Geschmacks verbessert (24). Die kleinste Schwankung des durchschnittlichen Fruchtgewichts der „Encore F1“ durch die Lichtquelle könnte auf eine Toleranz dieser Sorte gegenüber der Lichtqualität hindeuten. Dies entspricht der Überprüfung des Themas (25). Der Ertrag und die Qualität von Tomaten werden nicht nur von der Intensität des verwendeten Zusatzlichts beeinflusst, sondern auch von seiner Qualität. Die Ergebnisse zeigen, dass sich unter IND-Lampen ein geringerer Ertrag gebildet hat. Es ist jedoch möglich, dass aufgrund der geringeren Intensität von Induktionslampen geringere Ergebnisse erzielt werden, obwohl das Hauptmerkmal von Induktionslampen ein breiteres grünes Wellenband ist. Die Daten zeigen, dass die Erhöhung der Rotlichtmenge zur Erhöhung des Frischgewichts der Tomaten beiträgt, aber die Erhöhung des Trockensubstanzgehalts nicht beeinflusst. Es scheint, dass das rote Licht die Erhöhung des Wassergehalts in den Tomaten stimuliert hat. Im Gegensatz dazu reduziert die Zunahme an blauem Licht den Trockensubstanzgehalt aller Tomatensorten. Am wenigsten empfindlich ist die gelbe Tomatensorte „Balzano“. Mehrere Untersuchungen haben gezeigt, dass die Photosynthese unter einer Kombination aus rotem und blauem Licht tendenziell höher ist als unter HPS-Beleuchtung, der Fruchtertrag jedoch gleich ist (12). Olle und Virsil (26) fanden heraus, dass rote LEDs den Tomatenertrag erhöhen, und dies unterstreicht die Ergebnisse unserer Forschung, die besagt, dass im Allgemeinen eine höhere Zugabe von roten Wellen den Ertrag erhöht. Einer ähnlichen Meinung sind Zhang et al. (14) definiert, dass selbst das Hinzufügen von FR-Licht in Kombination mit roten LEDs und HPSL die Gesamtfruchtzahl erhöht. Zusätzliches blaues und rotes LED-Licht führte zu einer frühen Reifung der Tomatenfrucht. Dies könnte auf den Grund für eine höhere Fruchtmasse unter LEDs bei den Sorten „Chocomate F1“ und „Diamont F1“ hindeuten, da eine frühe Reifung zu einem früheren Ansatz neuer Früchte führte. In Bezug auf den Ertrag zeigen unsere Daten, dass nicht die Zunahme an rotem Licht für die Ertragssteigerung wichtiger ist, sondern der erhöhte Anteil an rotem Licht gegenüber blauem Licht.
Da eine der beliebtesten Eigenschaften der Tomate der Verbraucher die Süße ist, ist es wichtig, die Möglichkeiten zur Verbesserung dieser Eigenschaft zu verstehen. Dennoch wird es normalerweise durch verschiedene Umweltfaktoren verändert (27). Es gibt Hinweise darauf, dass die qualitative Zusammensetzung des Lichts auch den biochemischen Inhalt von Tomatenfrüchten beeinflusst. Lösliche Zuckergehalte der reifen Tomatenfrucht wurden durch längere FR-Lichtdauern verringert (15). Konget al. (16) Die Ergebnisse zeigten, dass die Behandlung mit blauem Licht signifikant zu mehr löslichen Feststoffen führte. Der Zuckergehalt in Pflanzen wird durch grünes, blaues und rotes Licht erhöht (28). Unsere Experimente bestätigen dies nicht, da die getrennte Erhöhung sowohl des blauen als auch des roten Lichts in den meisten Fällen den Gehalt an löslichen Feststoffen verringerte. Unsere Ergebnisse zeigten, dass der höchste Gehalt an löslichem Zucker unter HPSL gefunden wurde, das den größten Anteil an rotem Licht als andere Lampen bringt und auch die Temperatur in der Nähe der Lampen erhöht. Dies entspricht früheren Untersuchungen, bei denen Studien von Erdberga et al. (29) zeigten, dass der Gehalt an löslichen Zuckern und organischen Säuren mit zunehmender Dosis der roten Wellen zunimmt. Ähnliche Ergebnisse wurden in anderen Studien erhalten. Bei Pflanzen, die zusätzlich mit HPS-Lampen beleuchtet wurden, wurde ein höheres mittleres Tomatenfruchtgewicht erzielt als bei Pflanzen mit LED-Lampen (8.7-12.2 % je nach Sorte). (30).
Studien von Dzakovich et al. (31) bewiesen, dass die zusätzliche Lichtqualität (HPSL über LEDs) die physikalisch-chemischen (Gesamtmenge an löslichen Feststoffen, titrierbarer Säure, Ascorbinsäuregehalt, pH-Wert, Gesamtphenole und prominente Flavonoide und Carotinoide) oder sensorischen Eigenschaften von im Gewächshaus angebauten Tomaten nicht signifikant beeinflusste. Dies zeigt, dass der Gehalt an löslichem Zucker in Früchten nicht nur durch einzelne Faktoren, sondern auch durch deren Kombinationen beeinflusst werden kann. Auch in unseren Versuchen konnten keine Regelmäßigkeiten zwischen Lichteinflüssen auf den Säuregehalt festgestellt werden. Insbesondere sollte sich die zukünftige Forschung nicht nur auf die Beziehung zwischen Art und Licht, sondern auch auf die Beziehung zwischen Sorte und Licht konzentrieren. Der Trockenmassegehalt war bei „Chocomate F1“ und „Strabena F1“ höher. Dies entspricht Kurina et al. (6), wo die rotbraunen Akzessionen im Durchschnitt mehr Trockenmasse ansammelten (6.46 %). Studien von Duma et al. (32) zeigten, dass beim Vergleich der Fruchtmasse und des TI beobachtet wird, dass ein höherer TI für kleinere oder größere Tomaten gilt. Experimente von Rodica et al. (23) zeigten, dass kirschrote und braunrot gefärbte Tomaten mehr lösliche Feststoffe enthalten. In dieser Studie wird betont, dass die Menge der den Fruchtgeschmack bestimmenden organischen Verbindungen vom Ertrag der Sorte abhängt.
Die Exposition gegenüber zusätzlicher roter und blauer LED-Beleuchtung erhöht die Lycopin- und в-Carotingehalt (13, 29, 33, 34). Dannehlet al. (12) Studien haben gezeigt, dass der Lycopin- und Luteingehalt in Tomaten um 18 und 142 % höher war, wenn sie der LED-Leuchte ausgesetzt waren. Jedoch, в-Carotingehalt war zwischen den Lichtbehandlungen nicht unterschiedlich. Ntagkaset al. (35) zeigte, dass Zeaxanthin, das Produkt von в-Carotin-Umwandlung, Anstieg der Tomatenfrüchte unter blauem und weißem Licht. In dieser Studie treffen diese Aussagen teilweise nur auf „Bozen F1“ zu, wo deutlich größere Mengen an Lycopin unter LED-Behandlung gefunden wurden, aber в-Carotin reagierte negativ auf diese Behandlung. Dies könnte auf genetische Merkmale zurückzuführen sein, da „Bolzano F1“ in dieser Studie nur eine orangefrüchtige Sorte ist. In anderen Studien mit rotfruchtigen und braunen Sorten wurde die höchste Menge an Lycopin und в-Carotin wurden unter Induktionslampen gefunden, die die Trends der Vorjahre nicht bestätigen (29). Unsere Experimente zeigten, dass der Lycopingehalt aller roten Fruchttomatensorten mit zunehmendem blauem Licht zunahm. Im Gegensatz dazu können Änderungen des Carotingehalts in verschiedenen Sorten keine Regelmäßigkeiten feststellen, die allen in den Experimenten verwendeten Tomatensorten gemeinsam sind. Diese Diskrepanz weist darauf hin, dass in Zukunft zusätzliche Tests des Subjekts erforderlich sind. Dasselbe Reaktionsmuster auf Licht aufgrund von Sortenmerkmalen wurde bei Mengen an Phenolen und Flavonoiden beobachtet. Alle Sorten mit roten und braunen Früchten zeigten bessere Ergebnisse unter IND-Lampen, während „Bolzano F1“ ohne signifikanten Unterschied mit höheren Ergebnissen auf HPSL- und LED-Lampen reagierte. Diese Studie deckt sich mit den Erkenntnissen von Kong: Die Blaulichtbehandlung führte signifikant zu einer höheren Konzentration einzelner phenolischer Verbindungen (Chlorogensäure, Kaffeesäure und Rutin) (16). Kontinuierliches rotes Licht signifikant erhöhtes Lycopin, в-Carotin, Gesamtphenolgehalt, Gesamtflavonoidkonzentration und antioxidative Aktivität in Tomaten (36). In unseren früheren Studien veränderten sich Flavonoide schwankend; daher sollten keine Auswirkungen der Lichtwellenlänge als signifikant vermerkt werden.
Die Menge an Phenolen stieg mit dem wachsenden Anteil von blauem Licht, das von LED-Lampen bereitgestellt wird (29), das deckt sich auch mit unserer Forschung. In den Arbeiten anderer Forscher wird erwähnt, dass die Exposition gegenüber UV- oder LED-Licht keinen Einfluss auf die Gesamtmenge der Phenolverbindungen hatte, obwohl beide Lichtbehandlungen dafür bekannt sind, die Expression einer Reihe von Genen zu modulieren, die an der Biosynthese von Phenolverbindungen und Carotinoiden beteiligt sind (36). Es sollte erwähnt werden, dass es ähnlich wie beim Gewicht der Frucht keine signifikanten Unterschiede in den chemischen Zusammensetzungen in „Encore F1“ aufgrund der Lichtbehandlung gibt. Dies erlaubt die Erklärung, dass die Sorte „Encore F1“ gegenüber der Lichtzusammensetzung tolerant sein könnte. Unsere Experimente bestätigen die Literaturdaten, dass die Synthese von Sekundärmetaboliten sowohl durch die quantitative Menge an blauem Licht als auch durch den erhöhten Anteil an blauem Licht im gesamten Beleuchtungssystem verstärkt wird.
Die erzielten Ergebnisse zeigen, dass die chemischen Bestandteile, einschließlich der säurelöslichen Zucker und deren Verhältnis, die für den charakteristischen Geschmack der Sorte verantwortlich sind, in erster Linie von der Genetik der Sorte abhängen. Der gute Geschmack von Tomaten zeichnet sich nicht nur durch die Kombination artspezifischer Farbstoffe und biologisch aktiver Substanzen aus, sondern auch durch deren Menge. Insbesondere das Verhältnis und die Menge an Säuren und Zuckern prägen den gesättigten und hochwertigen Geschmack. In dieser Studie beträgt die positive Korrelation zwischen löslichen Zuckern und titrierbaren Säuren ~0.4, was mit der Forschung von Hernandez Suarez korreliert, wo die positive Korrelation zwischen den beiden Indikatoren mit 0.39 festgestellt wurde (37). In Studien von Dzakovich et al. (31)wurden Tomaten auf Gesamtlöslichkeit, titrierbarer Säuregehalt, Ascorbinsäuregehalt, pH-Wert, Gesamtphenole und auffällige Flavonoide und Carotinoide profiliert. Ihre Studien zeigten, dass die Fruchtqualität von Gewächshaustomaten durch zusätzliche Lichtbehandlungen nur geringfügig beeinträchtigt wurde. Darüber hinaus zeigten Verbrauchersensorik-Paneldaten, dass Tomaten, die unter verschiedenen Beleuchtungsbehandlungen angebaut wurden, bei allen getesteten Beleuchtungsbehandlungen vergleichbar waren. Die Studie legte nahe, dass die dynamische Lichtumgebung, die Gewächshausproduktionssystemen innewohnt, die Auswirkungen der Lichtwellenlängen, die in ihren Studien auf bestimmte Aspekte des Sekundärstoffwechsels von Früchten verwendet wurden, zunichte machen kann (31). Dies stimmt teilweise mit dieser Studie überein, da die erhaltenen Zahlen keine klaren und eindeutigen Trends zeigen, die es uns erlauben zu sagen, dass eine der Beleuchtungen für Tomaten nützlicher ist als die anderen. Bestimmte Lampen können jedoch für bestimmte Sorten verwendet werden, z. B. wären HPSL-Lampen besser geeignet für „Bolzano F1“ und LED-Beleuchtung wird für „Chocomate F1“ empfohlen. Dies entspricht einer Studie, in der die Wirkung verschiedener geografischer Breiten auf die chemischen Eigenschaften von Tomaten untersucht wurde. Bhandari et al. (38) stellte klar, dass die Kombination aus dem Sonnenstand zum Himmel und folglich der Kombination aus sichtbaren Lichtwellen zwar eine wichtige Rolle bei der Veränderung der chemischen Zusammensetzung von Tomaten spielt; Es gibt Sorten, die gegen diese Prozesse immun sind. All diese Schlussfolgerungen erlauben es zu unterstreichen, dass die chemische Zusammensetzung der Tomate in erster Linie vom Genotyp abhängt, da die Beziehungen der Sorten zu Wachstumsfaktoren, insbesondere zur Beleuchtung, genetisch prädisponiert sind.
FAZIT
Verschiedene Tomatensorten reagieren unterschiedlich auf die eingesetzte Zusatzbeleuchtung. Die Sorten „Encore“ und „Strabena“ reagieren am wenigsten auf zusätzliches Licht. Bei „Encore“ ist der einzige Parameter, der signifikant vom LED-Lichtspektrum beeinflusst wird, der Gehalt an löslichen Feststoffen. „Strabena“ ist auch relativ tolerant gegenüber Änderungen in der spektralen Zusammensetzung des Lichts. Dies könnte auf die genetischen Eigenschaften der Sorte zurückzuführen sein, da dies die einzige Kirschtomatensorte war, die in den Versuch aufgenommen wurde. Es wird nicht empfohlen, orangefarbene Früchte der Sorte „Bolzano“ unter LED- oder IND-Lampen anzubauen, da bei dieser Beleuchtung die Parameter auf dem Niveau von HPSL oder deutlich schlechter sind. Unter LED-Lampen werden das Gewicht einer Frucht, Trockenmasse, Gehalt an löslichen Feststoffen und в-Carotin sind deutlich reduziert. Das eine Fruchtgewicht und die Menge an в-Carotin der rotbraunen Fruchtsorte „Chocomate“ unter LED-Beleuchtung deutlich erhöht. Andere Parameter, ausgenommen Trockenmasse und Gehalt an löslichen Feststoffen, sind ebenfalls höher als bei Früchten, die unter HPSL gewonnen wurden.
Experimente haben gezeigt, dass HPSL die Akkumulation von Primärmetaboliten in Tomatenfrüchten stimuliert. In allen Fällen war der Gehalt an löslichen Feststoffen um 4.7–18.2 % höher als bei anderen Lichtquellen.
Da LED- und IND-Lampen etwa 20 % blauviolettes Licht emittieren, deuten die Ergebnisse darauf hin, dass dieser Teil des Spektrums die Akkumulation von Phenolverbindungen in der Frucht um 1.6–47.4 % im Vergleich zu HPSL stimuliert. Der Gehalt an Carotinoiden als Sekundärmetaboliten hängt sowohl von der Sorte als auch von der Lichtquelle ab. Rote Fruchtsorten neigen dazu, mehr zu synthetisieren в-Carotin unter zusätzlichem LED- und IND-Licht.
Der blaue Teil des Spektrums spielt eine größere Rolle bei der Sicherstellung der Erntequalität. Eine Erhöhung bzw. Quantifizierung seines Anteils am Gesamtspektrum fördert die Synthese von Sekundärmetaboliten (Lycopin, Phenole und Flavonoide), was zu einer Abnahme des Trockensubstanz- und Trockensubstanzgehalts führt.
Angesichts des großen Einflusses der genotypischen Variabilität bei Tomaten und Lichtverhältnissen sollten sich weitere Studien weiterhin auf die Kombinationen von Sorten und verschiedenen zusätzlichen Lichtspektren konzentrieren, um den Gehalt an biologisch aktiven Verbindungen zu erhöhen.
DATENVERFÜGBARKEITSERKLÄRUNG
Die Rohdaten, die die Schlussfolgerungen dieses Artikels stützen, werden von den Autoren ohne unangemessenen Vorbehalt zur Verfügung gestellt.
AUTHOR BEITRÄGE
IE war für den Anbau und die Probenahme von Tomaten, die Laborarbeit und die Quantifizierung von Verbindungen verantwortlich und trug auch zum Schreiben des Manuskripts bei. IA brachte die Idee auf, trug zur Studienkonzeption und -design bei, war verantwortlich für die Probenentnahme von Tomaten, die Laborarbeit, die Quantifizierung von Verbindungen und trug auch zum Schreiben des Manuskripts bei. MD trug zur Studienkonzeption und -design bei, optimierte Analysemethoden, analysierte die Proben im Labor und gab Empfehlungen und Vorschläge. RA trug zur statistischen Analyse und Interpretation der Daten bei und machte Empfehlungen und Vorschläge zum Manuskript. LD trug zur Studienkonzeption und -design bei, war verantwortlich für die Probenentnahme von Tomaten, die Laborarbeit, die Quantifizierung von Verbindungen und gab Empfehlungen und Vorschläge zum Manuskript. Alle Autoren haben zum Artikel beigetragen und die eingereichte Version des Manuskripts genehmigt.
FINANZIERUNG
Diese Studie wurde vom lettischen Programm zur Entwicklung des ländlichen Raums 2014-2020 Zusammenarbeit finanziert, Aufruf 16.1, Projekt-Nr. 19-00-A01612-000010 Untersuchung innovativer Lösungen und Entwicklung neuer Methoden zur Effizienz- und Qualitätssteigerung im lettischen Gewächshaussektor (IRIS).
REFERENZEN
- 1. Vijayakumar A., Shaji S., Beena R., Sarada S., Sajitha Rani T., Stephen R., et al. Durch hohe Temperaturen induzierte Veränderungen in der Qualität und den Ertragsparametern von Tomaten (Solanum lycopersicum L) und Ähnlichkeitskoeffizienten zwischen Genotypen Verwendung von SSR-Markern. Heliyon. (2021) 7:e05988. doi: 10.1016/j.heliyon.2021.e0 5988
- 2. Duzen IV, Oguz E, Yilmaz R, Taskin A, Vuruskan A, Cekici Y, et al. Lycopin hat eine schützende Wirkung auf eine septische Schock-induzierte Herzverletzung bei Ratten. Bratisl Med J. (2019) 120:919-23. doi: 10.4149/BLL_2019_154
-
3. A. Dogukan, M. Tuzcu, CA. Agca, H. Gencoglu, N. Sahin, M. Onderci et al. Der Tomaten-Lycopin-Komplex schützt die Niere vor Cisplatin-induzierten Schäden, indem er oxidativen Stress sowie Bax, Bcl-2 und HSPs beeinflusst Ausdruck. Nutr Krebs. (2011) 63:427-34. doi: 10.1080/01635581.2011.5 35958
- 4. Warditiani NK, Sari PMN, Wirasuta MAG. Phytochemische und hypoglykämische Wirkung von Tomaten-Lycopin-Extrakt (TLE). Sys Rev. Pharm. (2020) 11:50914. doi: 10.31838/srp.2020.4.77
- 5. Ando A. „Geschmacksverbindungen in Tomaten“. In: Higashide T, Herausgeber. Solanum Lycopersicum: Produktion, Biochemie und Nutzen für die Gesundheit. New York, Nova Science Publishers (2016). p. 179-187.
- 6. Kurina AB, Solovieva AE, Khrapalova IA, Artemyeva AM. Biochemische Zusammensetzung von Tomatenfrüchten verschiedener Farben. Vavilovskii Zhurnal Genet Selektsii. (2021) 25:514-27. doi: 10.18699/VJ21.058
- 7. Murshed R, Lopez-Lauri F, Sallanon H. Wirkung von Wasserstress auf antioxidative Systeme und oxidative Parameter in Tomatenfrüchten (Solanum lycopersicon L, cvMicro-tom). Physiol Mol Biol Pflanzen. (2013) 19:36378. doi: 10.1007/s12298-013-0173-7
- 8. Klunklin W, Savage G. Wirkung von Qualitätsmerkmalen von Tomaten, die unter gut bewässerten und Trockenstressbedingungen angebaut werden. Lebensmittel. (2017) 6:56. doi: 10.3390/foods6080056
- 9. Chetelat RT, Ji Y. Zytogenetik und Evolution. Genetic Improv Solanaceous Crops. (2007) 2:77-112. doi: 10.1201/b10744-4
- 10. W. Wang, D. Liu, M. Qin, Z. Xie, R. Chen, Y. Zhang. Auswirkungen zusätzlicher Beleuchtung auf den Kaliumtransport und die Fruchtfärbung von in Hydrokultur angebauten Tomaten. Int. J. Mol. Sci. (2021) 22:2687. doi: 10.3390 / ijms22052687
- 11. Ouzounis T, Giday H, Kj^r KH, Ottosen CO. LED oder HPS in Zierpflanzen? Eine Fallstudie zu Rosen und Campanulas. Eur. J. Hortic Sci. (2018) 83:16672. doi: 10.17660/eJHS.2018/83.3.6
- 12. Dannehl D, Schwend T, Veit D, Schmidt U. Steigerung von Ertrag, Lycopin und Luteingehalt in Tomaten, die unter kontinuierlichem PAR-Spektrum angebaut werden LED-Beleuchtung. Front Plant Sci. (2021) 12:611236. doi: 10.3389/fpls.2021.61 1236
- 13. Xie BX, Wei JJ, Zhang YT, Song SW, Su W, Sun GW, et al. Zusätzliches blaues und rotes Licht fördert die Lycopinsynthese in Tomatenfrüchten. J Integrator Agric. (2019) 18:590-8. doi: 10.1016/S2095-3119(18)62062-3
- 14. Zhang JY, Zhang YT, Song SW, Su W, Hao YW, Liu HC. Zusätzliches Rotlicht führt je nach Ethylenproduktion zu einer früheren Reifung der Tomatenfrucht. Environ Exp-Bot. (2020) 175:10404. doi: 10.1016/j.envexpbot.2020.104044
- 15. Zhang Y, Zhang Y, Yang Q, Li T. Zusätzliches dunkelrotes Overhead-Licht stimuliert das Tomatenwachstum unter Beleuchtung innerhalb des Baldachins mit LEDs. J Integrator Agric. (2019)18:62-9. doi: 10.1016/S2095-3119(18)62130-6
- 16. Kong D, Zhao W, Ma Y, Liang H, Zhao X. Auswirkungen der Beleuchtung mit Leuchtdioden auf die Qualität von frisch geschnittenen Kirschtomaten während der Kühlung Lagerung. Int J Food Sci Technol. (2021) 56: 2041-52. doi: 10.1111/ijfs. 14836
- 17. Jarqum-Enriquez L, Mercado-Silva EM, Maldonado JL, Lopez-Baltazar J. Lycopingehalt und Farbindex von Tomaten werden durch das Gewächshaus beeinflusst Startseite. Sc Horticulturae. (2013) 155:43-8. doi: 10.1016/j.scienta.2013. 03.004
- 18. A. Wahid, S. Gelani, M. Ashraf, MR. Foolad. Hitzetoleranz
in Pflanzen: ein Überblick. Environ Exp-Bot. (2007) 61:199
223. doi: 10.1016/j.envexpbot.2007.05.011
- 19. Duma M, Alsina I. Der Gehalt an Pflanzenfarbstoffen in roten und gelben Paprika. Sci Pap B Gartenbau. (2012) 56:105-8.
- 20. Nagata M, Yamashita I. Einfache Methode zur gleichzeitigen Bestimmung von Chlorophyll und Carotinoiden in Tomatenfrüchten. J Jpn Food Sci Technol. (1992) 39:925-8. doi: 10.3136/nskkk1962.39.925
- 21. Singleton VL, Orthofer R., Lamuela-Raventos RM. Analyse von Gesamtphenolen und anderen Oxidationssubstraten und Antioxidantien mittels Folin-Ciocalteu-Reagenz. Methoden Enzymol. (1999) 299: 152-78. doi: 10.1016/S0076-6879(99)99017-1
- 22. Kim D, Jeond S, Lee C. Antioxidative Kapazität von phenolischen sekundären Pflanzenstoffen aus verschiedenen Pflaumensorten. Lebensmittelchem. (2003) 81:321-6. doi: 10.1016/S0308-8146(02)00423-5
- 23. Rodica S, Maria D, Alexandru-Ioan A, Marin S. Die Entwicklung einiger Ernährungsparameter der Tomatenfrucht während der Erntephasen. Hort Sci. (2019) 46:132-7. doi: 10.17221/222/2017-HORTSCI
- 24. Mate MD, Szalokine Zima I. Entwicklung und Ertrag von Feldtomate bei unterschiedlicher Wasserversorgung. Res. J. Agric Sci. (2020) 52:167-77.
- 25. Mauxion JP, Chevalier C, Gonzalez N. Komplexe zelluläre und molekulare Ereignisse, die die Fruchtgröße bestimmen. Trends Plant Sci. (2021) 26:1023-38. doi: 10.1016/j.tplants.2021.05.008
- 26. Olle M, Alsina I. Einfluss der Lichtwellenlänge auf Wachstum, Ertrag und Nährwert von Gewächshausgemüse. Proc Lettisch Acad Sci B. (2019) 73:1-9. doi: 10.2478/prolas-2019-0001
- 27. K. Kawaguchi, R. Takei-Hoshi, I. Yoshikawa, K. Nishida, M. Kobayashi, M. Kushano et al. Die funktionelle Störung des Zellwand-Invertase-Inhibitors durch Genom-Editierung erhöht den Zuckergehalt von Tomatenfrüchten ohne Fruchtgewicht verringern. Sci Rep. (2021) 11:1-12. doi: 10.1038/s41598-021-00966-4
- 28. Olle M, Virsile A. Einfluss der Lichtwellenlänge auf Wachstum, Ertrag und Ernährungsqualität von Gewächshausgemüse. Agricult Food Sci. (2013) 22:22334. doi: 10.23986/afsci.7897
- 29. I. Erdberga, I. Alsina, L. Dubova, M. Duma, D. Sergejeva, I. Augspole, et al. Veränderungen in der biochemischen Zusammensetzung von Tomatenfrüchten unter dem Einfluss der Beleuchtungsqualität. Key Eng Mater. (2020) 850:172
- 30. Gajc-Wolska J, Kowalczyk K, Metera A, Mazur K, Bujalski D, Hemka L. Wirkung der Zusatzbeleuchtung auf ausgewählte physiologische Parameter und den Ertrag von Tomatenpflanzen. Folia Horticulturae. (2013) 25:153
-
9. doi: 10.2478/kurz-2013-0017
- 31. M. Dzakovich, C. Gomez, MG Ferruzzi, CA Mitchell. Die chemischen und sensorischen Eigenschaften von Gewächshaustomaten bleiben als Reaktion auf rotes, blaues und fernrotes zusätzliches Licht von Lichtemittern unverändert. Gartenwissenschaft. (2017) 52:1734-41. doi: 10.21273/HORTSCI12469-17
- 32. Duma M, Alsina I, Dubova L, Augspole I, Erdberga I. Anregungen für Verbraucher zur Eignung verschiedenfarbiger Tomaten in der Ernährung. Im:
FoodBalt 2019: Proceedings of 13th Baltic Conference on Food Science and Technology; 2019 2.-3. Mai. Jelgava, Lettland: LLU (2019). p. 261-4.
- 33. Ngcobo BL, Bertling I, Clulow AD. Die Beleuchtung von Kirschtomaten vor der Ernte verkürzt die Reifezeit, verbessert die Carotinoidkonzentration in der Frucht und die Gesamtfruchtqualität. J. Hortic Sci. Biotechnol. (2020) 95:617–27. doi: 10.1080/14620316.2020.1743771
- 34. Najera C, Guil-Guerrero JL, Enriquez LJ, Alvaro JE, Urrestarazu
M. LED-verbesserte diätetische und organoleptische Eigenschaften in
Tomatenfrucht nach der Ernte. Postharvest Biol Technol. (2018)
145:151-6 . doi: 10.1016/j.postharvbio.2018.07.008
- 35. Ntagkas N, de Vos RC, Woltering EJ, Nicole C, Labrie C, Marcelis L F. Modulation ofthe tomato fruit metabolome byLED light. Metaboliten. (2020) 10:266. doi: 10.3390/metabo10060266
- 36. N. Baenas, C. Iniesta, R. Gonzalez-Barrio, V. Nunez-Gomez, M. J. Periago, F. J. Garda-Alonso. Verwendung von ultraviolettem Licht (UV) und Leuchtdioden (LED) nach der Ernte zur Verbesserung bioaktiver Verbindungen gekühlte Tomaten. Moleküle. (2021) 26:1847. doi: 10.3390/molecules260 71847
- 37. Hernandez Suarez M., Rodriguez ER, Romero CD. Analyse des Gehalts an organischen Säuren in auf Teneriffa geernteten Tomatensorten. Eur Food Res Technol. (2008) 226:423-35. doi: 10.1007/s00217-006-0553-0
- 38. Bhandari HR, Srivastava K, Tripathi MK, Chaudhary B, Biswas S. Shreya Environmentx Kombinieren der Fähigkeitsinteraktion für Qualitätsmerkmale bei Tomaten (Solanum lycopersicum L.). Int J Bio-Resour Stress Manage. (2021) 12:455-62. doi: 10.23910/1.2021.2276
Interessenkonflikt: Die Autoren erklären, dass die Forschung ohne kommerzielle oder finanzielle Beziehungen durchgeführt wurde, die als potenzieller Interessenkonflikt ausgelegt werden könnten.
Anmerkung des Herausgebers: Alle in diesem Artikel geäußerten Ansprüche sind ausschließlich die der Autoren und stellen nicht notwendigerweise die ihrer angeschlossenen Organisationen oder des Herausgebers, der Herausgeber und der Rezensenten dar. Alle Produkte, die in diesem Artikel bewertet werden, oder Behauptungen, die von ihrem Hersteller aufgestellt werden, werden vom Herausgeber nicht garantiert oder unterstützt.
Copyright © 2022 Alsina, Erdberg, Duma, Alksnis und Dubova. Dies ist ein Open-Access-Artikel, der unter den Bedingungen der Creative Commons Attribution License (CC BY) verbreitet wird.
Neue Möglichkeiten im Bereich Ernährung | www.frontiersin.org